Tache de vin
Tache de vin
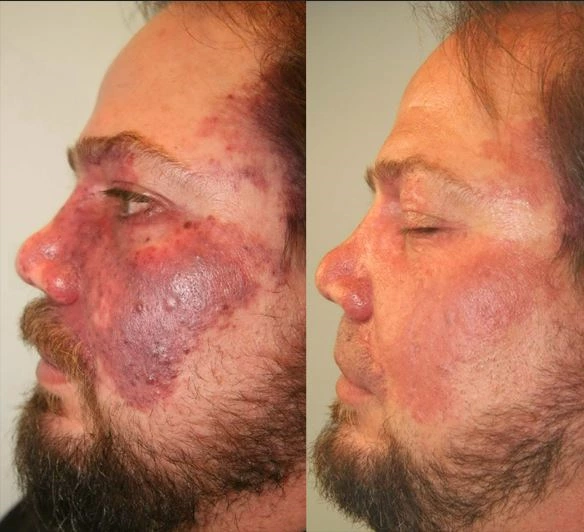
Tache de vin (PWS)
La tache de vin (TPV) , également appelée nævus flammeus ou malformation capillaire, est une plaque relativement plate et rarement surélevée composée de capillaires dilatés. Il s'agit d'une malformation capillaire congénitale.
Étiologie et pathogénèse
L'étiologie et la pathogénèse du SPW sont inconnues. On pense généralement qu'il résulte d'erreurs dans l'expression génétique, la traduction ou la synthèse des protéines au cours du développement embryonnaire, avec des facteurs génétiques impliqués. Il apparaît généralement à la naissance ou peu de temps après et grandit proportionnellement au corps, sans jamais régresser. L'incidence est de 0,3 % à 0,5 % chez les nouveau-nés. Le SPW est généralement sporadique, mais des cas familiaux ont été signalés, avec une transmission autosomique dominante. Certains patients développent le SPW plus tard dans la vie, peut-être déclenché par un traumatisme, des contraceptifs oraux ou une exposition prolongée au soleil. Les capillaires des lésions sont dilatés mais ont des cellules endothéliales normales, et la coloration immunohistochimique ne peut pas les distinguer des capillaires dermiques normaux. Cependant, la coloration de la protéine S100 montre une réduction significative des terminaisons nerveuses sympathiques dans les vaisseaux dermiques superficiels, ce qui peut être lié à des changements de tension vasculaire et de dilatation capillaire.
Manifestations cliniques
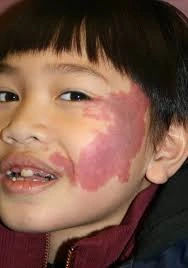
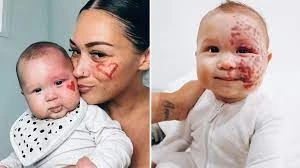
Le syndrome de Prader-Willi survient généralement chez les nourrissons ou les enfants, avec des taux similaires chez les hommes et les femmes. Les lésions apparaissent souvent sur le visage, le cou et le cuir chevelu, généralement unilatérales mais parfois bilatérales, et touchent parfois les muqueuses. La plupart des syndromes de Prader-Willi sont très superficiels, avec une profondeur moyenne de 0,46 mm. Les nouvelles lésions se présentent sous forme de plaques rouges bien définies, qui peuvent apparaître n'importe où sur le corps, mais 90 % se produisent sur la tête et le cou, en particulier dans les première et deuxième branches du nerf trijumeau. Au début, les lésions sont roses et deviennent progressivement rouge foncé ou violettes avec l'âge. Le changement de couleur n'est pas lié à la profondeur ou à l'épaisseur des vaisseaux. Au fil du temps, les vaisseaux deviennent tortueux et dilatés, épaississant les lésions et donnant un aspect pavé, formant parfois des nodules. Des études montrent qu'à l'âge de 46 ans, environ les deux tiers des patients développent un épaississement de la peau et la formation de nodules, commençant généralement vers 37 ans. Les nodules peuvent facilement s'ulcérer et saigner. Même dans la petite enfance, le PWS peut développer des granulomes pyogènes. Les lésions persistent généralement toute la vie et régressent rarement spontanément. Le PWS peut également provoquer une hypertrophie de la peau sous-jacente, des tissus mous et des os.
Outre les problèmes esthétiques, le syndrome de PWS peut être associé à un glaucome (avec une probabilité de 45 % s'il touche la branche supérieure du nerf trijumeau), à une ulcération, à des saignements et à des infections secondaires. Environ 9,5 % des patients atteints de syndrome de PWS facial présentent des anomalies oculaires ou du système nerveux, les lésions plus importantes étant plus susceptibles d'entraîner des complications systémiques.
Sous vidéomicroscopie in vivo, le PWS présente deux types : (1) des boucles vasculaires tortueuses, superficielles et dilatées (type spot) ; (2) des plexus vasculaires superficiels, parallèles et dilatés (type ring). Certaines lésions présentent des caractéristiques des deux types. Le premier type répond mieux au traitement au laser à colorant pulsé, tandis que le second type est plus profond et présente des vaisseaux de connexion entre les plexus vasculaires dilatés et parallèles.
Caractéristiques pathologiques
Au microscope, les lésions du syndrome de PWS présentent des capillaires dilatés regroupés et des cellules endothéliales matures dans le derme supérieur et moyen. La dilatation capillaire augmente avec l'âge et peut s'étendre au derme profond et au tissu sous-cutané sans prolifération de cellules endothéliales. Les vaisseaux sont entourés de fibres de collagène lâches et la lumière est remplie de globules rouges. Dans la petite enfance, il n'y a pas d'anomalies significatives ; à l'âge adulte, seule une dilatation vasculaire sous-papillaire est observée.
Diagnostic et diagnostic différentiel
Le diagnostic repose sur la présence de taches rouges ou rouge foncé à la naissance ou apparaissant peu de temps après, s'agrandissant avec la croissance corporelle et ne régressant pas spontanément.
Le diagnostic différentiel comprend :
- Hémangiome congénital précoce : Le diagnostic nécessite l'observation de la progression des lésions, généralement rapide dans les hémangiomes.
- Tache de vin infantile : également appelée nævus simple, nævus flammeus ou malformation capillaire médiane, touchant souvent le front, le nez, la lèvre supérieure, le cuir chevelu occipital ou les paupières. Généralement rose pâle, elle s'estompe ou disparaît généralement vers l'âge de 1 à 2 ans, à l'exception des lésions situées sur la ligne médiane du front ou dans la région sacrée.
Traitement
- Traitement chirurgical : Pour les hémangiomes plus volumineux ou les tumeurs vasculaires viscérales.
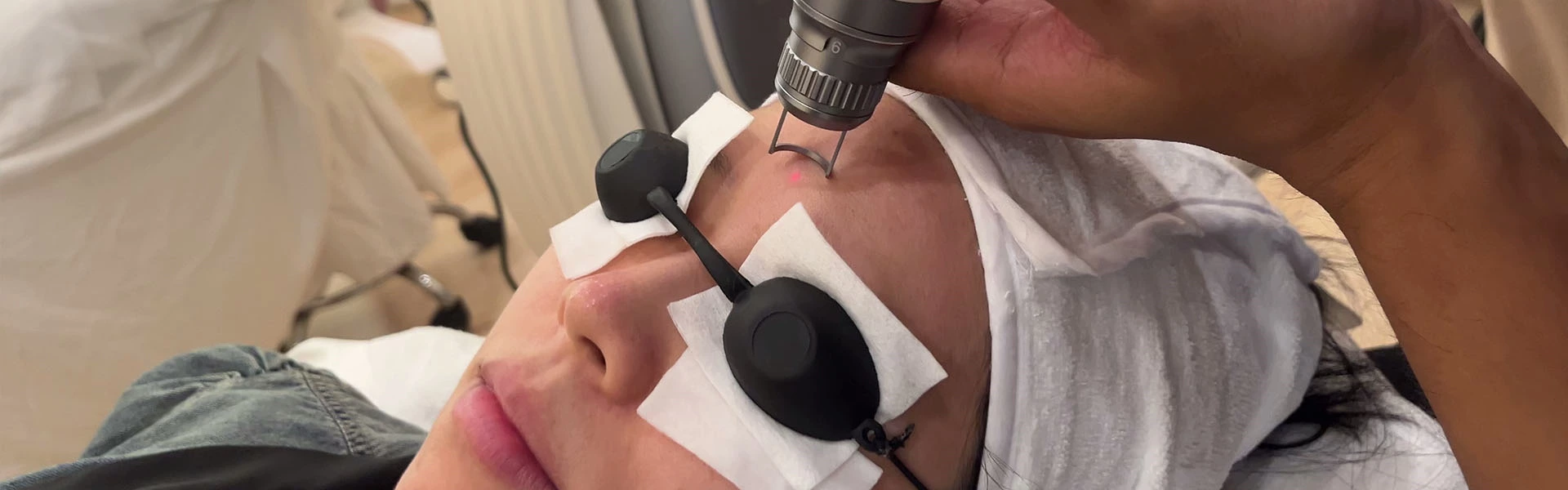
- Traitement au laser :
- Laser à colorant pulsé (PDL) : la référence absolue pour le traitement du PWS, avec des longueurs d'onde de 577 nm, 585 nm ou 595 nm, absorbée sélectivement par l'oxyhémoglobine avec un minimum de dommages aux autres composants épidermiques. Bien que le pic d'absorption optimal de l'oxyhémoglobine soit de 420 nm, cette longueur d'onde pénètre trop profondément pour atteindre les vaisseaux dermiques. Par rapport à 585 nm, 595 nm a une spécificité d'absorption moindre mais pénètre plus profondément, ce qui le rend adapté aux vaisseaux plus profonds. Les durées d'impulsion varient généralement de 0,45 à 40 ms, les vaisseaux fins chez les enfants étant mieux traités avec une durée d'impulsion de 0,5 ms et les vaisseaux plus gros avec des impulsions plus longues. La densité énergétique est généralement de 5 à 10 J/cm2. Pour soulager la douleur, des anesthésiques topiques peuvent être appliqués avant le traitement. Les critères d'évaluation du traitement sont une coloration plus foncée des lésions et un purpura, avec des effets secondaires courants tels que des cloques, une hyperpigmentation post-inflammatoire, une hypopigmentation, une sensibilité cutanée et des cicatrices. Le PDL est particulièrement efficace pour les petits capillaires chez les enfants, mais moins efficace pour les lésions prolifératives ou nodulaires. Les études montrent un taux d'amélioration moyen de 75 % après 2,5 traitements. En général, 5 à 10 traitements permettent d'obtenir une disparition ou une amélioration, les lésions superficielles répondant plus rapidement, atteignant une amélioration de 95 % après 1 à 2 traitements. Les adultes répondent moins favorablement, avec environ 20 % de résistance au traitement et un taux d'amélioration au premier traitement d'environ 50 %. Les avantages du traitement précoce comprennent une amélioration plus rapide, moins de séances de traitement, une zone de lésion plus petite et des besoins en anesthésie moindres.
- Laser Nd : efficace pour les lésions PWS résistantes ou hypertrophiées avec une pénétration plus profonde et des durées d'impulsion plus longues (1064 nm). Bien que similaire en termes d'absorption aux lasers 585 nm, le laser 1064 nm a un coefficient d'absorption et de diffusion absolu plus faible. Les lésions PWS se situent généralement 3 à 5 mm sous le derme, hors de portée du PDL, ce qui rend les longueurs d'onde plus longues viables. Les lasers Nd à impulsions longues provoquent rarement du purpura mais peuvent entraîner des cloques et des cicatrices. Les durées d'impulsion typiques sont de 10 à 50 ms, avec des densités d'énergie de 40 à 120 J/cm2, des intervalles de traitement de 1 à 2 mois et 4 à 10 séances nécessaires.
- Laser à double longueur d'onde : combinaison de lasers PDL et Ndlasers à impulsions longues, où la longueur d'onde du PDL correspond étroitement au pic d'absorption de l'oxyhémoglobine mais a une efficacité limitée pour les vaisseaux profonds et de grande taille en raison de sa longueur d'onde plus courte et de sa pénétration superficielle. Les lasers à double longueur d'onde utilisent un mode d'émission séquentielle, émettant d'abord du PDL pour convertir l'oxyhémoglobine en méthémoglobine, suivi du laser Ndlaser, améliorant considérablement la spécificité et l'efficacité du traitement tout en réduisant le purpura et les cicatrices. Les combinaisons typiques sont des durées d'impulsion PDL de 0,25 à 10 ms, des densités d'énergie de 4 à 9 J/cm2 ; des durées d'impulsion laser 1064 nm de 15 à 40 ms, des densités d'énergie de 20 à 60 J/cm2, avec des intervalles de sortie de 500 à 1000 ms et des intervalles de traitement de 6 à 8 semaines, ajustés en fonction des caractéristiques de la lésion et de la réponse au traitement. Un refroidissement continu par air et des anesthésiques topiques (par exemple, crème à 2 % de lidocaïne + 2 % de prilocaïne) sont nécessaires. Les effets indésirables comprennent la douleur, l'érythème, l'œdème, la formation de cloques, l'hypopigmentation et la cicatrisation.
- Laser Nd à fréquence doublée : une option pour le PWS récurrent, avec une longueur d'onde plus courte (532 nm) limitant la profondeur de pénétration et provoquant davantage d'effets secondaires, tels que des changements de pigmentation transitoires et des cicatrices, en raison d'une absorption élevée de mélanine. Il est recommandé pour le PWS réfractaire avec des durées d'impulsion appropriées pour éviter le purpura.
- Lumière pulsée intense (IPL) : une lumière pulsée à large spectre avec une bonne efficacité, notamment pour les lésions résistantes au PDL. Les paramètres du système LumenisOne comprennent un traitement à impulsion unique avec des filtres 560 nm/590 nm/640 nm, des durées d'impulsion de 4 à 10 ms, des densités d'énergie de 12 à 22 J/cm2, un traitement à double impulsion avec des filtres 560 nm/590 nm, des durées d'impulsion de 3,5 à 4,0 ms, des densités d'énergie de 17 à 30 J/cm2 et des intervalles d'impulsion de 20 à 33 ms, avec des traitements toutes les 20 à 40 ms.
Soins de la peau après le traitement au laser Après un traitement au laser, la barrière cutanée est compromise, ce qui nécessite des soins de la peau post-traitement appropriés et des produits de soins médicaux appropriés pour réparer la peau endommagée.
- Réduction de l'érythème et de l'exsudation : En fonction de la réaction cutanée immédiate après le traitement, utilisez des masques contenant des ingrédients anti-inflammatoires et hydratants ou des compresses froides avec des sacs de glace enveloppés dans de la gaze. Si la peau devient blanche après le traitement, des compresses froides pendant environ 30 minutes sont recommandées ; pour une congestion et une rougeur normales, 15 minutes suffisent, en évitant les frottements. En cas d'érythème, de gonflement ou de saignement important, utilisez des compresses froides contenant une solution d'acide borique à 3 % ou une solution de furaciline à 5 %.
- Réduction de la réponse inflammatoire et prévention des infections : pour prévenir l'infection de la plaie postopératoire, appliquez une pommade à la mupirocine, une pommade à l'érythromycine ou des injections de gentamicine par voie topique. Pour les zones de traitement étendues et l'inflammation sévère, la prednisone orale 10 mg trois fois par jour pendant trois jours peut renforcer les effets anti-inflammatoires.
- Favorise la cicatrisation des plaies : Le facteur de croissance basique des fibroblastes (BFGF) est un mitogène important qui favorise la cicatrisation des plaies, la réparation et la régénération des tissus. Après le traitement au laser, appliquez le gel BFGF ou vaporisez-le uniformément sur la plaie pour favoriser la cicatrisation.
- Favoriser la régénération et la réparation de la peau : La reconstruction de la structure cutanée normale et la restauration des fonctions physiologiques sont essentielles en raison des différents degrés de dommages causés à la barrière lipidique de la peau, à la couche cornée, à l'aquaporine, à la structure de la paroi de briques et à la couche basale. Il est essentiel d'utiliser des produits de soin médicaux adaptés ayant des effets anti-inflammatoires et hydratants pendant 3 à 6 mois après le traitement.
- Protection solaire : Portez un chapeau de soleil, des vêtements en coton à manches longues et utilisez un parapluie (de préférence anti-UV) lorsque vous êtes à l'extérieur. Appliquez une crème solaire avec un FPS élevé (supérieur à 30) et une protection UVA (PFA ++ ou plus). Évitez toute exposition prolongée au soleil entre 10 h et 16 h. Des crèmes solaires efficaces et hautement sûres sont nécessaires pour prévenir les changements de pigmentation post-laser.
Autres traitements
- Radiothérapie : L’utilisation d’une irradiation aux rayons X peu profonde permet de traiter efficacement les hémangiomes capillaires.
- Cryothérapie : La cryothérapie à l'azote liquide, adaptée à la taille et à la forme des lésions, est principalement utilisée pour les hémangiomes capillaires, mais elle peut provoquer des cicatrices.
- Thérapie photodynamique : une option de traitement émergente pour le syndrome de Prader-Willi, qui pourrait devenir l'orientation future. Elle consiste à injecter un photosensibilisateur dans le sang, formant une concentration élevée dans les vaisseaux, puis à utiliser une longueur d'onde spécifique de lumière laser pour produire des espèces réactives de l'oxygène, provoquant des lésions des cellules endothéliales et la destruction de la paroi vasculaire tout en épargnant les tissus environnants. Des photosensibilisateurs comme les dérivés de l'hématoporphyrine (HpD) ou l'éther monométhylique d'hématoporphyrine (HMME) sont utilisés après un test cutané. L'HpD ou l'HMME est injecté par voie intraveineuse à raison de 4,5 à 5,5 mg/kg, suivi d'une irradiation laser. Les intervalles de traitement sont généralement d'environ un mois, l'HpD-PDT nécessitant une éviction de la lumière pendant un mois et l'HMME-PDT nécessitant 1 à 2 semaines. Idéal pour les lésions roses chez les enfants, moins efficace pour les lésions épaisses et violettes, et comporte un risque de cicatrices en cas d'exposition prolongée au laser. Le HMME-PDT présente des réactions postopératoires plus douces, des périodes de guérison plus courtes, une plus grande sécurité et des périodes d'évitement de la lumière plus courtes par rapport au HpD-PDT.
Ressources supplémentaires
Source: Tache de vin

 Laser Ciillulu - Fournisseur de machines pour le visage
Laser Ciillulu - Fournisseur de machines pour le visage